-
流感是一种严重的上呼吸道病毒感染,由于其高毒力和突变率,该病毒仍然是对公众健康的主要威胁。据美国疾病控制与预防中心和世界卫生组织估计,每年有多达65 万人死于季节性流感引起的呼吸道疾病[1]。传统中医药预防和治疗流感病毒导致的感染(如呼吸道肺炎和支气管炎)已成为中国临床上常规治疗策略,发挥了独特的医疗优势[2,3]。
感冒安颗粒是由金银花、连翘、板蓝根、拳参、桑叶、紫苏和荆芥等七味中药制成的复方制剂,临床应用30 多年,具有疏散风邪,解表退热功能,其预防和治疗呼吸道感染的作用已得到很好的临床验证,特别是在病毒感染初期的治疗效果尤其显著,但药效物质基础并不清楚。目前,建立了TLC法对方中的板蓝根和连翘两味药材进行特征鉴别;同时对方中各药味的共有成分绿原酸和齐墩果酸也建立了TLC鉴别方法。在含量限度方面,则建立了制剂中连翘酯苷A的HPLC法。尽管这些获批的标准已用于制剂常规质量控制,但尚需进一步进行质量评价,以期更客观、准确地反映感冒安颗粒的临床疗效。
由于中药复方复杂的化学成分,它的药理作用是通过多靶点、多途径而实现的。流感病毒感染的病理生理过程主要是病毒的直接作用和宿主免疫反应损伤(如细胞因子风暴所致的炎性损伤和ROS导致的氧化应激损伤)的结果[2,4]。为了研究感冒安颗粒临床效果的药效物质基础,我们对组方各药味的化学成分进行了文献追踪,发现方中药味含有多种黄酮类成分,如异槲皮苷、芦丁、木樨草素及木樨草苷等[5-9]。而黄酮类成分对流感病毒的作用越来越受到关注[10,11]。异槲皮苷抑制流感病毒A和B的复制,与抗病毒药amantadine或者oseltamivir合用可抑制它们导致的耐药病毒出现[12]。槲皮素与流感病毒A H1N1(A/PR/8/34)的神经酰胺酶的结合与zanamivir相当,体内研究也证实了其抗流感病毒能力,可作为抗甲型H1N1流感的有效先导化合物[13]。Zima研究认为木犀草素及其同源物是强效流感核酸内切酶抑制剂,揭示黄酮类化合物的抗流感作用[14]。鉴于此,本研究在总黄酮含量测定的基础上[15],采用HPLC-MS/MS方法建立5 种黄酮类成分的定量方法,不仅为制剂质量评价提供方法学,也为进一步研究感冒安颗粒防治流感病毒引起的呼吸道感染机制奠定物质基础。
-
Agilent Technologies
6410 Triple Quad LC/MS仪,配以Triple Quad B.02.01(B2043.12)数据处理软件(美国安捷伦公司);XS205DU电子天平(瑞士梅特勒-托利多仪器有限公司);DL-720A超声波清洗器(上海之信仪器有限公司)。 -
感冒安颗粒(本院院内制剂,批号110418、110704、111025、111121、111130、111221、120131、120201、120207、120214);芦丁对照品(中国食品药品检定研究院,供UV法测定,含量以92.5 %计,批号:100080-200707);金丝桃苷对照品(中国食品药品检定研究院,供含量测定用,含量以93.9 %计,批号:111521-201004);木犀草素对照品(中国食品药品检定研究院,供含量测定用,批号:111520-200504);槲皮素对照品(中国食品药品检定研究院,供含量测定用,批号:100081-200406);异槲皮苷对照品(成都曼斯特生物制品有限公司,纯度>99.0 %,批号:MUST-10021901);甲醇为色谱纯;甲酸为分析纯;水为蒸馏水。
-
分别取芦丁、金丝桃苷、异槲皮苷、槲皮素和木犀草素对照品各适量,用甲醇溶解,摇匀,各配制成500 μg/ml的对照品贮备液。分别精密量取5种对照品贮备液适量,稀释成浓度如下:分别含芦丁0.25、0.50、1.00、2.00、4.00、6.00、8.00 μg/ml,金丝桃苷0.002、0.008、0.020、0.032、0.044、0.056、0.080 μg/ml,异槲皮苷0.03、0.10、0.25、0.45、0.65、0.95、2.00 μg/ml,槲皮素0.02、0.10、0.20、0.30、0.40、0.60、0.70 μg/ml,木犀草素0.012、0.026、0.040、0.054、0.082、0.096、0.200 μg/ml的混合对照品溶液。
-
按已优化的黄酮提取方法进行[15]。取样品约0.5 g,精密称定,置量瓶中,加70 %甲醇35 ml,超声提取30 min,放冷,过滤,滤液加70 %甲醇溶液定容至50 ml,摇匀,用微孔滤膜(0.45 μm)滤过,即得。
-
色谱条件:采用Kromasil C 18(4.6 mm×150 mm,5 μm,100 Å)色谱柱;甲醇(A)- 0.1 %甲酸(B)作为流动相,按0~20 min,35 % A;20~40 min,45 % A梯度洗脱。
质谱条件:电喷雾负离子化(ESI−)源:毛细管电压 3.0 kV;气体温度 350 ℃,气体流速 10 L/min,雾化气压 35 psi。多反应模式(MRM)监测。5种黄酮检测的离子对:芦丁m/z 609.1→300.1、金丝桃苷和异槲皮苷m/z 463.0→300.1、槲皮素m/z 301.0→151.0、木犀草素m/z 285.0→132.9。
-
采用上述色谱条件,每个待测化合物对照品用70%甲醇溶液进行系列稀释,分别以信噪比(S/N)等于3和10确定各自的检测限和定量限。结果见表1。
表 1 5种黄酮成分的线性方程、相关系数、线性范围、检测限和定量限
黄酮化合物 线性方程 相关系数
r线性范围
(ng/ml)检测限
(ng/ml)定量限
(ng/ml)芦丁 Y=24 527X–162.17 0.999 7 250~8 000 0.025 0.50 金丝桃苷 Y=34 123X– 1.7381 0.999 1 2~80 0.005 0.01 异槲皮苷 Y=29 935X+1 597.80 0.999 1 30 ~2 000 0.02 0.50 槲皮素 Y=19 667X+370.71 0.999 2 20~700 0.02 0.10 木犀草素 Y=33 076X–177.98 0.999 7 12~200 0.005 0.01 -
精密量取“2.1.1”项下配制的5 种黄酮成分的对照品混合溶液,照“2.2”项下进样测定,记录各待测组分的峰面积积分值。横坐标为黄酮成分质量浓度(X,ng/ml),纵坐标为峰面积(Y),进行线性回归,计算回归方程和相关系数。结果见表1,表明5 种黄酮成分在各自浓度范围内呈良好的线性关系。
-
精密吸取供试品溶液(批号
120131 ),照“2.2”项下操作,进样,连续测定5 次和连续测定5 d,记录各待测组分的峰面积积分值,计算日内、日间RSD。结果显示,芦丁、金丝桃苷、异槲皮苷、槲皮素和木犀草素的日内精密度RSD分别为1.09 %、1.42 %、1.69 %、0.86 %、1.27 %(n=5),日间精密度RSD分别为1.85 %、1.76 %、1.43 %、2.01 %、1.90 %(n=5),表明仪器精密度良好。 -
取同一批号样品(批号
120131 )5 份,各0.5 g,精密称定,照“2.1.2”项下方法制备供试品溶液,照“2.2”项下操作,进样,测定峰面积积分值,并进行含量测定。结果显示,芦丁、金丝桃苷、异槲皮苷、槲皮素和木犀草素的含量分别为260.16、1.84、19.76、13.39、3.73 μg/g(n=5),RSD分别为1.51 %、1.73 %、0.90 %、1.44 %、1.68 %(n=5),表明方法的重复性良好。 -
取已知含量的样品(批号120131)9 份,每份约0.5 g,精密称定,各精密加入对照品贮备液适量,使已知样品中加入的相当对照品量分别含芦丁140.00 μg、金丝桃苷0.90 μg、异槲皮苷10.00 μg、槲皮素7.00 μg、木犀草素1.90 μg的各对照品贮备液,按“2.1.2”项下的方法制备供试品溶液,照“2.2”项下操作,进样,测定峰面积积分值,计算加样回收率。结果显示,芦丁、金丝桃苷、异槲皮苷、槲皮素和木犀草素的平均加样回收率分别为:102.06%、101.60%、100.63%、102.81%、101.80%(n=9),RSD分别为1.56%、1.93%、0.67%、2.07%、1.84%(n=9)。
-
取10 个批号的感冒安颗粒,分别按“2.1.2”项下的方法制备供试品溶液,照“2.2”项下操作,进样,测定峰面积积分值,计算含量,结果见表2。
表 2 不同批号感冒安颗粒含量测定结果(
$\bar x $ ±s, n=3)批号 芦丁 金丝桃苷 异槲皮苷 槲皮素 木犀草素 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 110418 479.83±1.99 0.41 0.855±0.004 0.49 20.54±0.25 1.23 14.83±0.05 0.31 3.46±0.06 1.70 110704 198.98±3.01 1.52 0.596±0.006 1.05 11.79±0.20 1.68 15.31±0.13 0.86 4.51±0.01 0.19 111025 32.23±0.26 0.83 0.993±0.012 1.26 13.31±0.00 0.02 6.53±0.04 0.55 5.15±0.08 1.58 111121 69.18±1.03 1.51 0.499±0.006 1.26 13.36±0.21 1.56 8.04±0.14 1.69 5.65±0.07 1.19 111130 67.53±0.27 0.40 0.533±0.008 1.57 13.36±0.21 1.54 7.48±0.12 1.62 5.42±0.06 1.15 111221 275.38±3.61 1.31 0.291±0.002 0.73 11.44±0.02 0.21 15.74±0.02 0.14 6.51±0.02 0.24 120131 264.55±0.51 0.19 1.825±0.012 0.68 20.29±0.04 0.17 13.66±0.02 1.52 3.78±0.01 0.26 120201 239.19±1.55 0.65 0.593±0.010 1.76 18.95±0.06 0.33 18.41±0.21 1.16 3.86±0.03 0.81 120207 109.20±2.14 1.97 0.503±0.004 0.83 18.00±0.21 1.16 6.72±0.08 1.22 4.21±0.02 0.37 120214 108.93±0.59 0.54 0.461±0.002 0.45 17.67±0.10 0.01 6.32±0.08 1.19 4.73±0.01 0.11 -
为了获得良好的MS结果,优化了检测的离子模式、碎裂电压、碰撞能量等参数,以获得高灵敏度的分子离子和碎片离子。结果显示,ESI采用负离子模式可使待测的黄酮成分有更高的灵敏度。对照品混合液经产物离子扫描显示,芦丁的主要碎片为m/z:300.1、271.0;金丝桃苷和异槲皮苷的主要碎片为m/z:300.1、270.8;槲皮素的主要碎片为m/z:178.6、151.0、120.9、106.9;木犀草素的主要碎片为m/z:150.9、132.9、106.8。依据定量碎片离子选择原则,从远离母离子、裂解方式稳定、碎片离子有足够的丰度等方面进行考察,最终选择的碎裂电压、碰撞能量和定量离子如表3所示。由于金丝桃苷和异槲皮苷是结构异构体,它们有相同分子离子峰[M-H]− m/z 463,MS/MS图谱中有相同的产物离子峰m/z 300,这两个化合物通过比较两者在HPLC中的保留时间进行定位。
表 3 5种黄酮化合物的质谱检测参数
黄酮化合物 母离子 产物离子 碰撞电压
(U/ V)碰撞能量
(U/ eV)芦丁 609.1 300.1 190 38 金丝桃苷 463.0 300.1 170 25 异槲皮苷 463.0 300.1 170 25 槲皮素 301.0 151.0 130 19 木犀草素 285.0 132.9 150 37 -
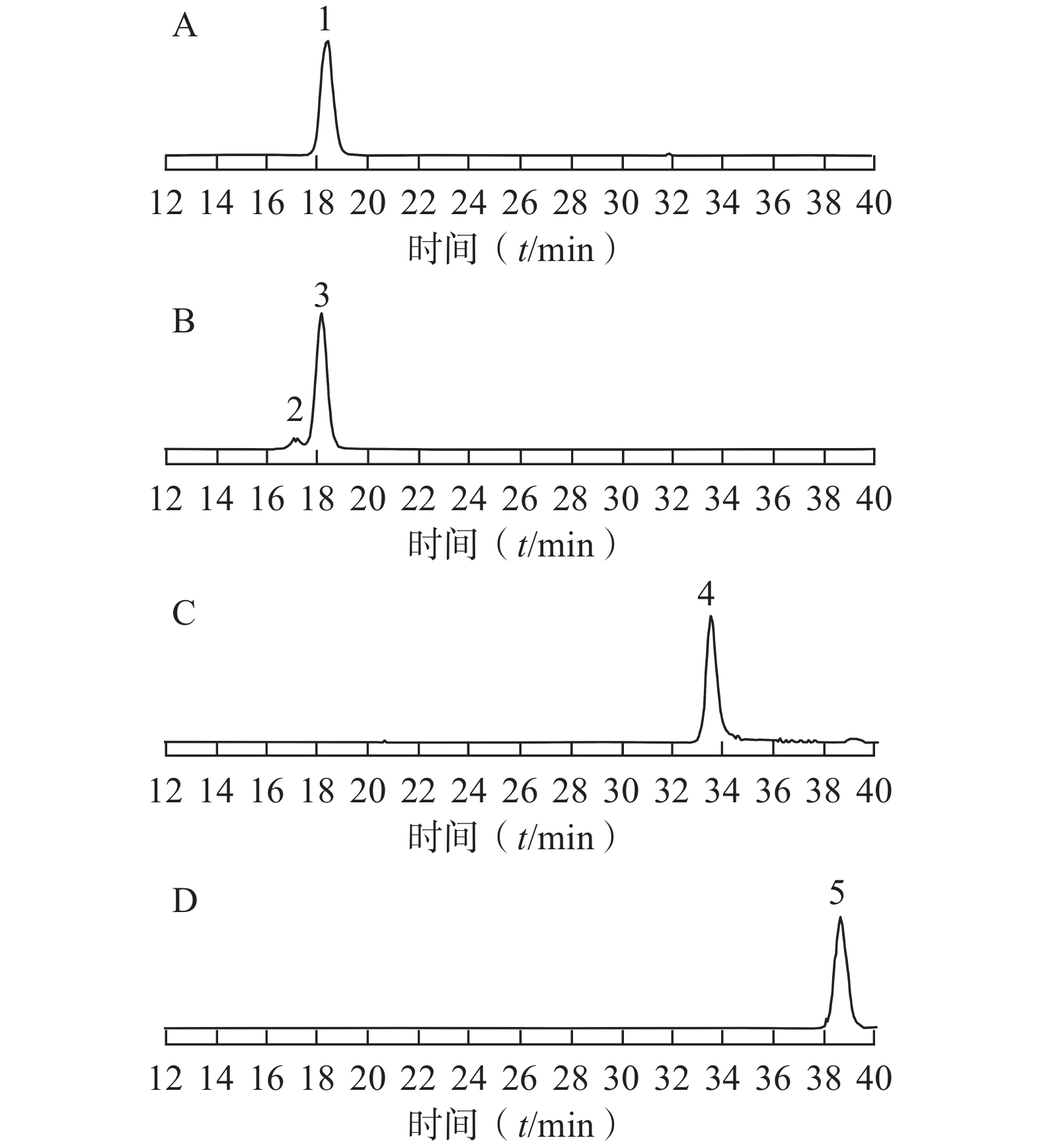
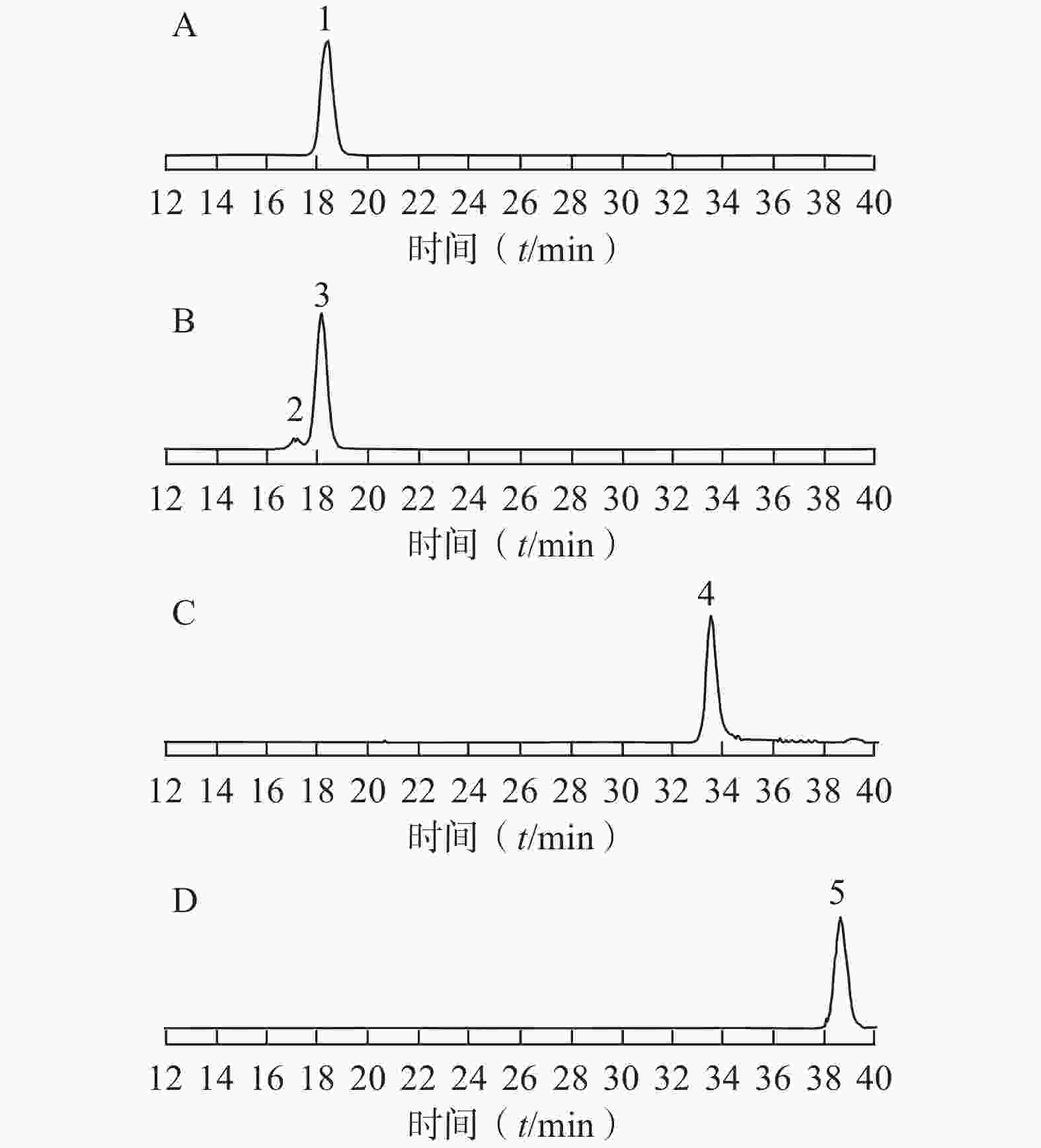
采用已优化的测定条件,感冒安颗粒中5 种黄酮类成分通过与各自标准对照品的保留时间和MS谱图的比较得以鉴别和确认,结果见图1。由于金丝桃苷、异槲皮苷和芦丁均是以槲皮素为苷元,结合不同的糖而形成,金丝桃苷与异槲皮苷还具有相同的分子量,它们的保留时间非常相近。采用HPLC-UV或二极管阵列检测的方法专属性不强,待测成分间相互干扰,很难保证测定结果的准确性。而本研究采用MS/MS-MRM模式测定,实现了准确定量的目的。
-
本研究采用经优化的超声提取法提取感冒安颗粒中黄酮成分,用所建立的LC-MS/MS方法测定了10 个批号样品,结果显示,每批样品中均为芦丁含量最高,金丝桃苷含量最低;批间样品同种黄酮成分含量存在差异。为了保证感冒安颗粒质量的稳定性,临床疗效的一致性,对其中的主要黄酮成分可以考虑设定最低限度要求。感冒安颗粒是经传统水提醇沉工艺制得的稠膏制粒而成,我们以往的研究表明,制剂中含有大量的酸性成分[16],工艺提取过程中的高温、偏低的pH值可能导致金丝桃苷、异槲皮苷、芦丁等苷类黄酮化合物发生水解反应。本研究将3种黄酮苷对照品及生产工艺获得的稠膏经2 % HCl溶液在80 ℃水浴加热处理30 min,进行HPLC-MS/MS分析,处理后的稠膏样品中金丝桃苷和芦丁含量降低,异槲皮苷和槲皮素含量增加;在3种黄酮苷对照品水解液中,均有槲皮素产生;除此之外,芦丁对照品溶液水解还出现了异槲皮苷。由此可以推测,感冒安颗粒的制备工艺可能导致黄酮类成分的水解和转化。
本研究采用HPLC-MS/MS同时测定了感冒安颗粒中5 种黄酮类成分的含量,所建立方法的专属性、灵敏度、精密度和准确性均已得到确证,达到了同时测定多种结构相似的黄酮类成分的目的,为其质量标准的建立提供了方法学依据。我们的研究已经证明感冒安颗粒中含有多种酚酸类成分[17],本研究又测定了其中的黄酮类成分。这些成分可能共同作用于流感病毒在宿主内复制的多环节,或者改善流感病毒对机体的炎性损伤,降低炎性细胞因子表达,改善氧化应激损伤,提高机体的免疫力等,充分发挥其多途径和多靶点作用优势,为其预防和治疗流感病毒所致呼吸道感染性疾病奠定物质基础。
Simultaneous determination of five flavonoids in Ganmao’an granules by HPLC-MS/MS
-
摘要:
目的 建立HPLC-MS/MS方法测定感冒安颗粒中5 种黄酮成分含量。 方法 色谱条件:色谱柱为Kromasil C18柱(4.6 mm×150 mm×4.6 mm,5 μm,100 Å),流动相为甲醇(A)-0.1 %甲酸(B),梯度洗脱(0~20 min,35% A;20~40 min,45% A),流速为1.0 ml/min,柱温为25 ℃;质谱条件:电喷雾电离源(ESI源)负离子扫描,多反应监测(MRM)模式检测。5种黄酮检测的离子对:芦丁m/z 609.1→300.1、金丝桃苷和异槲皮苷m/z 463.0→300.1、槲皮素m/z 301.0→151.0、木犀草素m/z 285.0→132.9。 结果 5个成分在一定浓度范围内与峰面积具有良好的线性关系,相关系数r均>0.999 1;平均加样回收率在100.63 %~102.81 %之间,RSD范围在0.67 %~2.07 %。10 批感冒安颗粒中芦丁、金丝桃苷、异槲皮苷、槲皮素和木犀草素的含量测定结果分别为32.23~479.83、0.291~1.825、11.44~20.54、6.32~18.41、3.46~6.51 μg/g。 结论 建立的HPLC-MS/MS法灵敏度高、专属性强,适合同时测定感冒安颗粒中5 种黄酮类成分的含量。 Abstract:Objective To develop a high performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) method for simultaneous determination of five flavonoids in Ganmao’an granules (GMA). Methods Chromatographic separation was achieved on a Kromasil C18 Column (150 mm× 4.6 mm,5 μm,100 Å), which was eluted with methanol (A)-0.1 % formic acid (B) at the flow rate of 1.0 ml/min. The gradient condition was as follows: 0-20 min, 35% A, and 20-40 min, 45% A. The column temperature was 25 °C. Analytes were detected using a triple quadrupole tandem mass spectrometer equipped with an electrospray ionization source in the negative ion scanning. The multiple reaction monitoring mode was used for qualitative analysis. For each flavonoid, two precursor ion/product ion transitions were chosen: lutin m/z 609.1→300.1, hyperin and isoquercitrin m/z 463.0→300.1, quercetin m/z 301.0→151.0, luteolin m/z 285.0→132.9. Results Five flavonoids showed the good relationships within their own concentration ranges (correlation coefficient r>0.999 1), whose average recoveries were in the range of 100.63 %-102.81 % with RSDs of 0.67 %-2.07 %. The content results of rutin, hyperoside, isoquercetin, quercetin, and luteolin in 10 batches of GMA were 32.23-479.83, 0.291-1.825, 11.44-20.54, 6.32-18.41, 3.46-6.51 μg/g, respectively. Conclusion The results indicated that the developed method was sensitive, accurate and could provide excellent specificity for simultaneous determination of five flavonoids in GMA. -
Key words:
- HPLC-MS/MS /
- Ganmao’an granules /
- rutin /
- hyperin /
- isoquercitrin /
- quercetin /
- luteolin
-
表 1 5种黄酮成分的线性方程、相关系数、线性范围、检测限和定量限
黄酮化合物 线性方程 相关系数
r线性范围
(ng/ml)检测限
(ng/ml)定量限
(ng/ml)芦丁 Y=24 527X–162.17 0.999 7 250~8 000 0.025 0.50 金丝桃苷 Y=34 123X– 1.7381 0.999 1 2~80 0.005 0.01 异槲皮苷 Y=29 935X+1 597.80 0.999 1 30 ~2 000 0.02 0.50 槲皮素 Y=19 667X+370.71 0.999 2 20~700 0.02 0.10 木犀草素 Y=33 076X–177.98 0.999 7 12~200 0.005 0.01 表 2 不同批号感冒安颗粒含量测定结果(
$\bar x $ ±s, n=3)批号 芦丁 金丝桃苷 异槲皮苷 槲皮素 木犀草素 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 含量(μg/g) RSD(%) 110418 479.83±1.99 0.41 0.855±0.004 0.49 20.54±0.25 1.23 14.83±0.05 0.31 3.46±0.06 1.70 110704 198.98±3.01 1.52 0.596±0.006 1.05 11.79±0.20 1.68 15.31±0.13 0.86 4.51±0.01 0.19 111025 32.23±0.26 0.83 0.993±0.012 1.26 13.31±0.00 0.02 6.53±0.04 0.55 5.15±0.08 1.58 111121 69.18±1.03 1.51 0.499±0.006 1.26 13.36±0.21 1.56 8.04±0.14 1.69 5.65±0.07 1.19 111130 67.53±0.27 0.40 0.533±0.008 1.57 13.36±0.21 1.54 7.48±0.12 1.62 5.42±0.06 1.15 111221 275.38±3.61 1.31 0.291±0.002 0.73 11.44±0.02 0.21 15.74±0.02 0.14 6.51±0.02 0.24 120131 264.55±0.51 0.19 1.825±0.012 0.68 20.29±0.04 0.17 13.66±0.02 1.52 3.78±0.01 0.26 120201 239.19±1.55 0.65 0.593±0.010 1.76 18.95±0.06 0.33 18.41±0.21 1.16 3.86±0.03 0.81 120207 109.20±2.14 1.97 0.503±0.004 0.83 18.00±0.21 1.16 6.72±0.08 1.22 4.21±0.02 0.37 120214 108.93±0.59 0.54 0.461±0.002 0.45 17.67±0.10 0.01 6.32±0.08 1.19 4.73±0.01 0.11 表 3 5种黄酮化合物的质谱检测参数
黄酮化合物 母离子 产物离子 碰撞电压
(U/ V)碰撞能量
(U/ eV)芦丁 609.1 300.1 190 38 金丝桃苷 463.0 300.1 170 25 异槲皮苷 463.0 300.1 170 25 槲皮素 301.0 151.0 130 19 木犀草素 285.0 132.9 150 37 -
[1] NACHBAGAUER R, PALESE P. Is a Universal Influenza Virus Vaccine Possible? Annu Rev Med[J]. 2020, 27(71): 315-327. [2] XIONG Y B, LI N X, DUAN N F, et al. Traditional Chinese medicine in treating influenza: from basic science to clinical applications[J]. Front Pharmacol, 2020, 11:575803. doi: 10.3389/fphar.2020.575803 [3] PENG Y Y, CHEN Z, LI H M, et al. Traditional Chinese medicine injections combined with oseltamivir for influenza: systematic review and network meta-analysis[J]. Front Pharmacol, 2022, 13:848770. doi: 10.3389/fphar.2022.848770 [4] YANG M R, WANG Y, YUE Y M, et al. Traditional Chinese medicines as effective agents against influenza virus-induced pneumonia[J]. Biomedecine Pharmacother, 2022, 153:113523. doi: 10.1016/j.biopha.2022.113523 [5] 国家药典委员会.中华人民共和国药典(一部)2020年版[S]. 北京: 中国医药科技出版社, 2020: 230. [6] WANG Z Y, XIA Q, LIU X, et al. Phytochemistry, pharmacology, quality control and future research of Forsythia suspensa (Thunb. )Vahl: a review[J]. J Ethnopharmacol, 2018, 210:318-339. doi: 10.1016/j.jep.2017.08.040 [7] 冯颖, 何俊, 刘虹, 等. 不同产地桑叶中6种化学成分含量的液相色谱-质谱联用同时测定[J]. 时珍国医国药, 2013, 24(3):572-574. doi: 10.3969/j.issn.1008-0805.2013.03.023 [8] 林闪闪, 王梦娇, 许金国, 等. 桑叶化学成分与药理作用研究进展及其质量标志物预测分析[J]. 中草药, 2023, 54(15):5112-5127. [9] 毛祈萍, 何明珍, 黄小方, 等. 基于超高效液相色谱和飞行时间质谱联用的紫苏化学成分鉴定[J]. 现代食品科技, 2021, 37(1):282-291,259. [10] PETRILLO A D, ORRÙ G, FAIS A, et al. Quercetin and its derivates as antiviral potentials: a comprehensive review[J]. Phytother Res, 2022, 36(1):266-278. doi: 10.1002/ptr.7309 [11] MORIMOTO R, HANADA A, MATSUBARA C, et al. Anti-influenza A virus activity of flavonoids in vitro: a structure-activity relationship[J]. J Nat Med, 2023, 77(1):219-227. doi: 10.1007/s11418-022-01660-z [12] KIM Y, NARAYANAN S, CHANG K O. Inhibition of influenza virus replication by plant-derived isoquercetin[J]. Antiviral Res, 2010, 88(2):227-235. doi: 10.1016/j.antiviral.2010.08.016 [13] LIU Z K, ZHAO J P, LI W C, et al. Computational screen and experimental validation of anti-influenza effects of quercetin and chlorogenic acid from traditional Chinese medicine[J]. Sci Rep, 2016, 6:19095. doi: 10.1038/srep19095 [14] ZIMA V, RADILOVÁ K, KOŽÍŠEK M, et al. Unraveling the anti-influenza effect of flavonoids: Experimental validation of luteolin and its congeners as potent influenza endonuclease inhibitors[J]. Eur J Med Chem, 2020, 208:112754. doi: 10.1016/j.ejmech.2020.112754 [15] 袁文琳, 宋洪杰, 高鸿彬, 等. 正交试验法优选感冒安颗粒总黄酮提取工艺[J]. 第二军医大学学报, 2012, 33(11):1272-1273. [16] 宋洪杰, 谢江, 高鸿彬, 等. 感冒安颗粒总有机酸含量测定方法的建立及应用[J]. 药学服务与研究, 2009, 9(4):298-300. doi: 10.3969/j.issn.1671-2838.2009.04.013 [17] 陈方剑, 宋洪杰, 高鸿彬, 等. 用HPLC法同时测定感冒安颗粒中没食子酸、绿原酸及咖啡酸的含量[J]. 药学服务与研究, 2012, 12(6):427-430. -



 下载:
下载: